Потенциометрический метод измерения низких концентраций натрия в деионизированной воде является наиболее чувствительным и распространенным методом. Однако определение низких концентраций натрия (менее 10 моль/дм3) сталкивается с рядом технических трудностей. Это задача специфическая и для ее решения требуется применение специальных приемов, и соблюдение определенных правил.
В первую очередь на погрешность измерений влияют т. н. «мешающие ионы». Концентрированный раствор KCl, истекающий из электрода сравнения, очень быстро увеличивает концентрацию ионов калия в пробе. Коэффициент селективности натрий-селективных измерительных электродов по отношению к ионам калия не очень велик и составляет ~10-2, и в результате анализатор начинает вместо ионов натрия реагировать на ионы калия. Поэтому такие измерения не могут быть выполнены обычным для потенциометрии способом - «в стакане». Их следует производить только при протоке пробы, для предотвращения накопления ионов калия в ячейке.
Другим «мешающим» ионом для любых натрий-селективных электродов является ион водорода. Для предотвращения его влияния в растворе необходимо поддерживать соотношение pH-pNa> 3...3.5. На практике pH анализируемой пробы независимо от содержания в ней натрия всегда доводят до значения 10... 10,5.
Для выполнения измерений низких концентраций натрия применяют специальные гидравлические устройства, которые обычно включают в себя систему регулирования расхода и стабилизации протока, устройство подщелачивания пробы и проточную измерительную ячейку.
Подщелачивание анализируемой пробы обычно осуществляется аммиаком, но могут использоваться и некоторые летучие амины. Прямое добавление раствора аммиака (или амина) в пробу недопустимо, т.к. при этом в нее неконтролируемо может быть внесен натрий. Поэтому подщелачивание осуществляется в специальных устройствах посредством насыщения пробы газообразным аммиаком.
Существует несколько способов подщелачивания пробы:
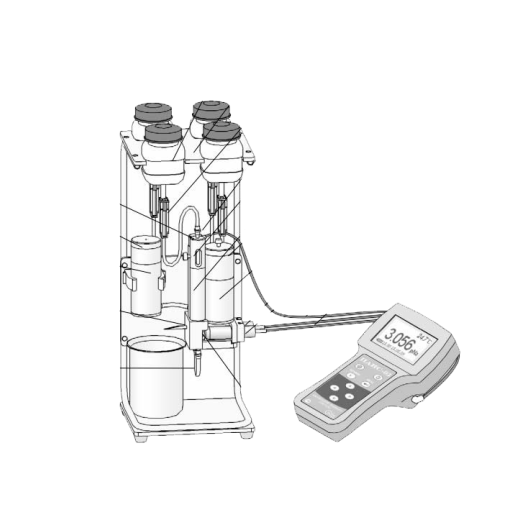
Рисунок 1 - Способы подщелачивания пробы при измерении концентрации ионов натрия в воде.
Другой проблемой при реализации метода является градуировка анализатора. Поскольку градуировка анализатора производится по градуировочным растворам, с которыми, в конечном счете, сравниваются анализируемые растворы, то погрешность их приготовления напрямую отразится на погрешности анализа. Особую сложность представляет градуировка анализатора, для определения малых концентраций натрия начиная с 1 мкг/дм3.
При приготовлении растворов с концентрацией менее 10-5 моль/дм3 требуется высокая аккуратность, и соблюдение специальных мер. В том числе:
Освободить от натрия воду очень сложно, и даже обессоленная вода может содержать 0,5 - 3 мкг/дм3Na+, поэтому фактическая концентрация натрия в градуировочных растворах всегда больше заданной на значение фоновой концентрации, которое неопределённо.
Поэтому производители в своих рекомендациях по градуировке анализаторов прибегают к различным ухищрениям. Чаще всего предлагается определить с помощью настроенного прибора концентрацию натрия в обессоленной воде и учесть ее при расчете концентрации полученных градуировочных растворов. Получается замкнутый круг. Чтобы настроить анализатор, нужно иметь настроенный прибор.
Другой вариант - использовать растворы с концентрацией, точность приготовления которых может быть обеспечена (от 100...200 мкг/дм3), а измерения проводить экстраполяцией более низких концентраций. Однако по метрологическим правилам наименьшую погрешность измерений можно достичь при условии, что диапазоны градуировки и измерений совпадают.
В анализаторе pNa-205.2MH (ООО «Измерительная техника»), используя интеллектуальные возможности микропроцессорном техники, метод градуировки позволяет частично решить указанную проблему. Для этого разработан математический аппарат и алгоритм градуировки анализатора.
Градуировка анализатора производится следующим образом:
Крутизну электродной характеристики анализатора S1 на диапазоне измерения исходная вода - первый раствор можно определить следующим образом:

Крутизну электродной характеристики анализатора S2 на диапазоне измерения первый раствор - второй раствор можно определить следующим образом:

Здесь MNa- молярная масса натрия, Ex, E1 и E2 - потенциалы электродной системы в исходной воде, первом и втором растворе соответственно.
Учитывая, что характеристика электрода ЭЛИС-212 Na, входящего в комплект анализатора, линейна в диапазоне измеряемых концентраций ионов натрия (3x10-8 - 1 мол/дм3), можно записать равенство:

или

По этому уравнению преобразователь рассчитывает значение xи учитывает его при определении градуировочных констант измерительной системы.
Таким образом, анализатор градуируется по растворам, в которых концентрации определяемого иона находятся вблизи границ диапазона измерения, и при этом учитывается содержание ионов в воде, используемой для приготовления этих растворов.
Задача организации, в особенности же начало повседневной работы по формированию позиции позволяет оценить значение систем массового участия. Значимость этих проблем настолько очевидна